网站维护
系统内容更新/升级中

药明康德分子检测实验室(WuXi Molecular Testing laboratory, WX-MTL) 自2013年首次运行,是美国美国病理学家学院(College of American Pathologist, CAP)认证的实验室,专注DNA及RNA分子测试,支持各类临床试验,尤其是抗病毒药物,在丙型及乙型肝炎病毒 (HCV & HBV) 新药的临床服务积累丰富经验。
CAP是美国非营利性临床实验室认可机构,致力于临床实验室步骤的标准化和改进,被广泛认为是实验室质量保证的领导者,其认证是保障临床测试质量和效率的必要措施。WX-MTL自2011年运行开始就得到GLP认证,并于2013年获得了临床实验室标准(CLIA)认证,2016年初又得到CAP认证。自此,WX-MTL严格按CAP标准进行实验室运行,项目管理,及人员培训,对每一个临床测试进行系统、全面、定量的确认 (validation),统一临床样品管理,严格执行相关的SOP及临床测试的国家法规制度。
迄今,WX-MTL已经和近30家全球企业合作(其中包括排名前10的制药公司的5家),2016年支持了8项临床试验,其中7项均为HBV或HCV的新药临床试验,相关的临床样品总数超过1300例,一个HCV新药在日本批准上市,一个在美国上市,另一个在中国获得批准上市,并得到客户服务奖,共同发表学术论文(图一)。

WX-MTL的实验室设计严格,分为四个操作区域,试剂制备、样品制备(同时是P2实验室)、PCR及PCR后操作,确保人流、物流的单向性(图二)。除了常规的分子生物学仪器,WX-MTL还配备了Qiasymphony核酸自动提取和QIAxcel核酸质控设备,罗氏COBAS®AmpliPrep和COBAS®TaqMan 48 Analyzer,7900HT定量PCR仪和3730xl基因分析仪(图三)。


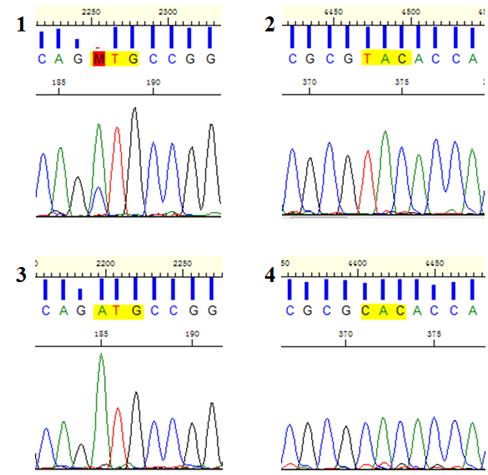
在HCV临床测试方面,WX-MTL可以支持病毒基因分型,IL28B基因分型,病毒RNA的Cobas定量,病毒单克隆测序,病毒基因(NS5A, NS5B, NS3/4A)耐药突变的一代测序分析(图四),病毒基因组的二代测序,SDM的表型分析,及病毒临床突变的表型分析。在HBV临床测试方面,WX-MTL可以进行以下检测:病毒基因分型,病毒DNA的Cobas定量,INNO-LiPA多重检测法分析核苷类似物治疗相关的突变,Pol-RT 基因一代测序,病毒全基因组的一代及二代测序,病毒临床突变的表型分析。从事HBV及HCV研发及临床测试的团队有30多位专门研究人员,所有临床测试人员都通过CAP的培训要求。
此外,WX-MTL还可以支持其它病毒(如流感病毒IFV,呼吸道合胞病毒RSV)的新药临床测试,药物基因组学测试,临床试验中相关基因的分型及突变测试,及MSI(微卫星不稳定)检测。